infos
sur la visualisation
des molécules
Les esters
Thierry Dulaurans
Lycée Pape Clément - Pessac
Connaître la fonction chimique ester,
savoir la reconnaître dans une molécule.
Écrire l' équation d'une estérificationet
nommer les esters simples.
Construire le premier paragraphe du cours (chapitre "estérification
et hydrolyse").
La structure électronique d'un atome permet de déterminer le nombre d'électrons externes de cet atome. On peut alors calculer, par soustraction, le nombre de liaisons covalentes que doit former cet atome.
| atome | H | C | O |
| numéro atomique Z | 1 | 6 | 8 |
| structure électronique | (K)1 | (K)2 (L)4 | (K)2 (L)6 |
| nombre d'électrons externes | 1 | 4 | 6 |
| règle à respecter | duet | octet | octet |
| nombre de liaisons covalentes formées |
1 | 4 | 2 |
Rappeler
le nombre de liaisons covalentes formées par :
- un atome d' hydrogène ;
-
un atome de carbone ;
- un atome d' oxygène.
Les
alcools sont des molécules qui possèdent un groupe hydroxyle ![]() .
.
On peut regrouper les
alcools en différentes classes.
Dans un alcool primaire l’atome de carbone fonctionnel est lié
au plus à un seul autre atome de carbone.
Dans un alcool secondaire l’atome de carbone fonctionnel est lié
à deux autres atomes de carbone.
Dans un alcool tertiaire l’atome de carbone fonctionnel est lié
à trois autres atomes de carbone.
Visualiser le méthanol, l’éthanol, le 2-méthylpropan-1-ol et le 2-méthylpropan-2-ol.
Écrire
la formule semi-développée, le nom et la classe de chacun de ces
alcools.
Dans ces formules, entourer le groupe fonctionnel.
Les acides carboxyliques
sont des molécules qui possèdent un groupe carboxyle![]() .
.
Visualiser l’acide éthanoïque et l' acide butanoïque.
Écrire
la formule semi-développée et le nom de chacun de ces acides carboxyliques.
Écrire la formule semi-développée et le nom de l' acide carboxylique comportant un seul atome de carbone.
Faire de même pour l' acide comportant trois atomes de carbone.
Dans ces formules, entourer le groupe fonctionnel.
Les
esters sont des molécules qui possèdent le groupe ester :
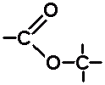 . . |
Recopier
la définition d'un ester.
La réaction d' estérification est la réaction entre un acide carboxylique et un alcool. Elle forme un ester et de l' eau.
Recopier la définition de l' estérification
Exemple :
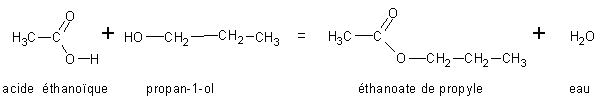
 |
|
Le nom d'un ester
comporte deux parties : |
Retour sur
l' exemple précédent :

Recopier l'exemple légendé de la réaction de formation de l'éthonoate de propyle et les règles de nomenclature.
butanoate
de méthyle méthanoate
de 1-méthylpropyle méthanoate
de 2-méthylpropyle
propanoate d'éthyle 2-méthylpropanoate
de méthyle éthanoate
d'éthyle
Recopier et compléter les équations ci-dessous. Nommer les molécules mises en jeu.
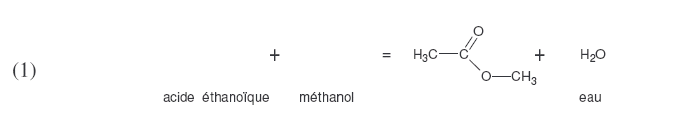 |
 |
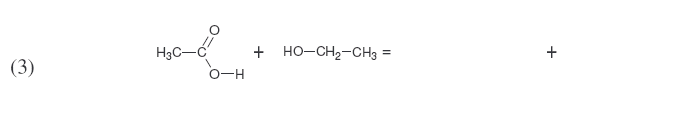 |
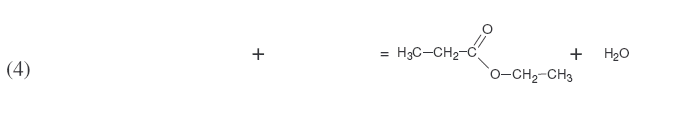 |
 |
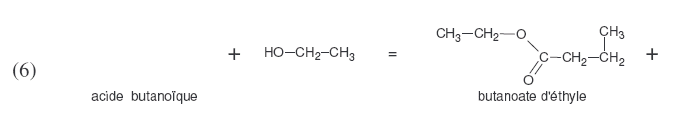 |
c' est fini